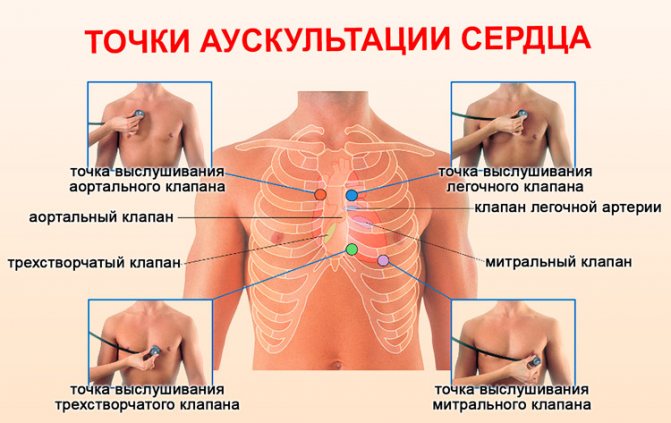
Содержание
Патология
Пороки развития П. с. с. могут возникать вследствие нарушения формирования межжелудочковой перегородки, при этом двойной контакт бульбовентрикулярного и атриовентрикулярного колец может привести к образованию двух (переднего и заднего) раздельных атриовентрикулярных узлов. Аномальные связи между другими специализированными мышечными кольцами приводят к возникновению ряда дополнительных проводящих структур, описанных в 1976 г. Венинком у некоторых животных и человека: ретроаортального узла, узлоподобных структур в межпредсердной перегородке, проводящих элементов атриовентрикулярного кольца. Исследования Андерсона (R. Н. Anderson) с соавт. (1977) показали, что нарушение нормальной связи предсердного и желудочкового миокарда при отделении атриовентрикулярного узла от одноименного пучка может привести к врожденной полной блокаде сердца, а наличие дополнительных проводящих путей (пучок Кента) между предсердиями и желудочками, идущих в обход атриовентрикулярного пучка, может способствовать развитию синдрома Вольффа — Паркинсона — Уайта (см. Вольффа-Паркинсона-Уайта синдром). При наличии пучка Джеймса, соединяющего миокард предсердия со стволом атриовентрикулярного пучка, или волокон Махейма, соединяющих ствол атриовентрикулярного пучка с миокардом желудочков, могут развиваться различные формы синдрома преждевременного возбуждения желудочков.
Приобретенная патология П. с. с. может возникать при функциональных или органических ее повреждениях (воспалении, ишемии, некрозе, дистрофии). В зависимости от уровня, степени и характера поражения П. с. с. развиваются различного типа нарушения нормальной координации сокращений между различными участками миокарда или отделами сердца (см. Аритмии сердца, Блокада сердца, Мерцательная аритмия, Пароксизмальная тахикардия, Сердце, патология, Экстрасистолия),
Библиография: Братанов В. С. Индивидуальные и возрастные особенности топографии предсердно-желудочковой проводящей системы человека, Вестн. хир., т. 105, № 10, с. 22, 1970; Михайлов С. С. и Ч укбар А. В. Топография элементов проводящей системы сердца человека, Арх. анат., гистол, и эмбриол., т. 44, № 6, с. 56, 1982; У м о-в и с т В. Н. Проводящая система при врожденных дефектах перегородок сердца, Киев, 1973, библиогр.; X у б у-тия Б. И., Ермолова 3. С. и Телятников С. С. Хирургическая анатомия проводящей системы сердца, Грудн. хир., № 1, с. 41, 1975; Ч е р в о-в а И. А. и Павлович Е. Р. Морфология основных отделов проводящей системы сердца крысы, Арх. анат., гистол, и эмбриол., т. 77, № 8, с. 67, 1979; А п-d er son R. Н. а. о. Congenitally complete heart block, developmental aspects, Circulation, v. 56, p. 90, 1977; В 1 о о г С. М. Cardiac pathology, Philadelphia, 1978; Brechenmacher C. Atrio-His bundle tracts, Brit. Heart J.* v. 37, p. 853, 1975; В u г с h e 1 1 H. B. In support of Kent, J. thorac. cardiovasc. Surg., v. 79, p. 637, 1980; The conduction system of the heart, Structure, function and clinical implications, ed. by H. J. Wel-lens a. o., p. 55, Leiden, 1976; D a-v i e s M. J. Pathology of conducting tissue of the heart, L., 1971; E 1 i s k a O. a. E 1 i s k о у a M. Venous circulation of the human cardiac conduction system, Brit. Heart J., v. 42, p. 508, 1979; они ж e, Lymphatic drainage of the ventricular conduction system in man and in the dog, Acta anat., v. 107, p. 205, 1980; Gardner E. a. O’ R a h i 1 1 у R. The nerve supply and conducting system of the human heart at the end of the embryonic period proper, J. Anat., v. 121, p. 571, 1976; Michailow S. Neue anatomische Forschungsergebnisse vom Nerven- und Reizleitungssystem des Herzens, S. 84, Stuttgart, 1974; Navaratnam V. The human heart and circulation, L.— N. Y., 1975; Osterwalder B. a. Schneider J. Morphologische Untersuchungen am menschlichen Reizleitungs, в кн.: Probleme der Medizin in der Ud SSR, hrsg. v. V. Parin u. L. Staroselsij, system, Schweiz, med. Wschr., S. 953, 1976; Sherf L. a. James Th. N. Fine structure of cells and their histologic organization within internodal pathways of the heart, clinical and electrocardiographic implications, Amer. J. Cardiol., v. 44, p. 345, 1979; Van der Hauwaert L. G., Stroobandt R. a. Yerhaeghe L. Arterial blood supply of the atrioventricular node and main bundle, Brit. Heart J., v. 34, p. 1045, 1972; Wenink A. C. G. Development of the human cardiac conducting system, J. Anat., v. 121, p. 617, 1976.
С. С. Михайлов, И. А. Червова.
Проводящая система сердца. Синусовый узел
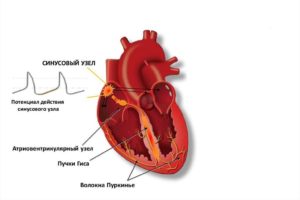
На рисунке показана схема проводящей системы сердца.
В ее состав входят: (1) синусный узел (который также называют синоатриальным или С-А узлом), где и происходит ритмическая генерация импульсов; (2) предсердные межузловые пучки, по которым импульсы проводятся от синусного узла к агриовентрикулярному узлу; (3) атриовентрикулярный узел, в котором происходит задержка проведения импульсов от предсердий к желудочкам; (4) атриовентрикулярный пучок, по которому импульсы проводятся к желудочкам; (5) левая и правая ножки А-В пучка, состоящие из волокон Пуркинье, благодаря которым импульсы достигают сократительного миокарда.
Синусный (синоатриальный) узел представляет собой небольшую эллипсовидную пластинку шириной 3 мм, длиной 15 мм и толщиной 1 мм, состоящую из атипических кардиомноцитов. С-А узел расположен в верхней части заднебоковой стенки правого предсердия у места впадения в него верхней полой вены.
Клетки, входящие в состав С-А узла, практически не содержат сократительных филаментов; их диаметр всего лишь 3-5 мкм (в отличие от предсердных сократительных волокон, диаметр которых 10-15 мкм).
Клетки синусного узла непосредственно связаны с сократительными мышечными волокнами, поэтому потенциал действия, возникший в синусном узле, немедленно распространяется на миокард предсердий.
Автоматия — это способность некоторых сердечных волокон самостоятельно возбуждаться и вызывать ритмические сокращения сердца. Способностью к автоматии обладают клетки проводящей системы сердца, в том числе клетки синусного узла. Именно С-А узел контролирует ритм сердечных сокращений, как мы увидим далее. А сейчас обсудим механизм автоматии.
Механизм автоматии синусного узла. На рисунке представлены потенциалы действия клетки синусного узла, записанные на протяжении трех сердечных циклов, и для сравнения — одиночный потенциал действия кардиомиоцита желудочка.
Необходимо отметить, что потенциал покоя клетки синусного узла имеет меньшую величину (от -55 до -60 мВ) в отличие от типичного кардиомиоцита (от -85 до -90 мВ). Это различие объясняется тем, что мембрана узловой клетки в большей степени проницаема для ионов натрия и кальция.
Вход этих катионов в клетку нейтрализует часть внутриклеточных отрицательных зарядов и уменьшает величину потенциала покоя.
Прежде чем перейти к механизму автоматии, необходимо вспомнить, что в мембране кардиомиоцитов существуют три типа ионных каналов, которые играют важную роль в генерации потенциала действия: (1) быстрые натриевые каналы, (2) медленные Na+/Са2+-каналы, (3) калиевые каналы.
Затем открываются калиевые каналы, происходит диффузия ионов калия из клетки — и мембранный потенциал возвращается к исходному уровню.
В клетках синусного узла потенциал покоя меньше, чем в клетках сократительного миокарда (-55 мВ вместо -90 мВ). В этих условиях ионные каналы функционируют по-другому. Быстрые натриевые каналы инактивированы и не могут участвовать в генерации импульса.
Дело в том, что любое уменьшение мембранного потенциала до -55 мВ на срок больший, чем несколько миллисекунд, приводит к закрытию инактивационных ворот во внутренней части быстрых натриевых каналов. Большая часть этих каналов оказывается полностью блокирована.
В этих условиях могут открыться только медленные Na+/Ca -каналы, и поэтому именно их активация становится причиной возникновения потенциала действия.
– Также рекомендуем “Самовозбуждение клеток синусного узла. Межузловые пучки сердца”
Оглавление темы “Проводящая система сердца. ЭКГ”: 1. Проводящая система сердца. Синусовый узел 2. Самовозбуждение клеток синусного узла. Межузловые пучки сердца 3. Физиология атриовентрикулярного узла. Проведение в волокнах Пуркинье 4. Распространение сердечного сокращения. Водитель ритма сердца 5. Эктопические водители ритма. Физиология системы Пуркинье и парасимпатической регуляции сердца 6. Влияние блуждающего нерва на сердце. Симпатическая регуляция сердца 7. Нормальная электрокардиограмма. ЭКГ – механизмы формирования 8. Зубцы электрокардиограммы. ЭКГ во взаимосвязи с сокращениями сердца 9. Распространение электрического тока вокруг сердца. Регистрация ЭКГ вокруг сердца 10. Электрокардиографические отведения. Треугольник и закон Эйнтховена
Функции проводящей системы сердца
Спонтанная генерация ритмических импульсов является результатом слаженной деятельности многих клеток синусно-предсердного узла, которая обеспечивается тесными контактами (нексусы) и электротоническим взаимодействием этих клеток. Возникнув в синусно-предсердном узле, возбуждение распространяется по проводящей системе на сократительный миокард.
Особенностью проводящей системы сердца является способность каждой клетки самостоятельно генерировать возбуждение. Существует так называемый градиент автоматии, выражающийся в убывающей способности к автоматии различных участков проводящей системы по мере их удаления от синусно-предсердного узла, генерирующего импульса с частотой до 60—80 в минуту.
В обычных условиях автоматия всех нижерасположенных участков проводящей системы подавляется более частыми импульсами, поступающими из синусно-предсердного узла. В случае поражения и выхода из строя этого узла водителем ритма может стать предсердно-желудочковый узел. Импульсы при этом будут возникать с частотой 40—50 в минуту. Если окажется выключенным и этот узел, водителем ритма могут стать волокна предсердно-желудочкового пучка (пучок Гиса). Частота сердечных сокращений в этом случае не превысит 30—40 в минуту. Если выйдут из строя и эти водители ритма, то процесс возбуждения спонтанно может возникнуть в клетках волокон Пуркинье. Ритм сердца при этом будет очень редким — примерно 20 в минуту.
Отличительной особенностью проводящей системы сердца является наличие в ее клетках большого количества межклеточных контактов — нексусов. Эти контакты являются местом перехода возбуждения с одной клетки на другую. Такие же контакты имеются и между клетками проводящей системы и рабочего миокарда. Благодаря наличию контактов миокард, состоящий из отдельных клеток, работает как единой целое. Существование большого количества межклеточных контактов увеличивает надежность проведения возбуждения в миокарде.
Возникнув в синусно-предсердном узле, возбуждение распространяется по предсердиям, достигая предсердно-желудочкового (атриовентрикулярного) узла. В сердце теплокровных животных существуют специальные проводящие пути между синусно-предсердным и предсердно-желудочковым узлами, а также между правым и левым предсердиями. Скорость распространения возбуждения в этих проводящих путях ненамного превосходит скорость распространения возбуждения по рабочему миокарду. В предсердно-желудочковом узле благодаря небольшой толщине его мышечных волокон и особому способу их соединения возникает некоторая задержка проведения возбуждения. Вследствие задержки возбуждение доходит до предсердно-желудочкового пучка и сердечных проводящих миоцитов (волокна Пуркинье) лишь после того, как мускулатура предсердий успевает сократиться и перекачать кровь из предсердий в желудочки.
Следовательно, атриовентрикулярная задержка обеспечивает необходимую последовательность (координацию) сокращений предсердий и желудочков.
Скорость распространения возбуждения в предсердно-желудочковом пучке и в диффузно расположенных сердечных проводящих миоцитах достигает 4,5—5 м/с, что в 5 раз больше скорости распространения возбуждения по рабочему миокарду. Благодаря этому клетки миокарда желудочков вовлекаются в сокращение почти одновременно, т. е. синхронно (см. рис. 7.2). Синхронность сокращения клеток повышает мощность миокарда и эффективность нагнетательной функции желудочков. Если бы возбуждение проводилось не через предсердно-желудочковый пучок, а по клеткам рабочего миокарда, т. е. диффузно, то период асинхронного сокращения продолжался бы значительно дольше, клетки миокарда вовлекались в сокращение не одновременно, а постепенно и желудочки потеряли бы до 50% своей мощности.
Таким образом, наличие проводящей системы обеспечивает ряд важных физиологических особенностей сердца: 1) ритмическую генерацию импульсов (потенциалов действия); 2) необходимую последовательность (координацию) сокращений предсердий и желудочков; 3) синхронное вовлечение в процесс сокращения клеток миокарда желудочков (что увеличивает эффективность систолы).
ЭКГ
Комплекс ЭКГ. P = зубец P, PR = интервал PR, QRS = комплекс QRS, QT = интервал QT, ST = сегмент ST, T = зубец T
Принцип формирования ЭКГ
Обратите внимание, что красные линии представляют волну деполяризации, а не кровоток.
Электрокардиограмма представляет собой запись электрической активности сердца.
Узел SA: зубец P
В нормальных условиях электрическая активность спонтанно генерируется узлом SA , кардиостимулятором. Этот электрический импульс распространяется через правое предсердие и через пучок Бахмана в левое предсердие , стимулируя сокращение миокарда предсердий. Проведение электрических импульсов по всему предсердию видно на ЭКГ , как Р — волна .
По мере того, как электрическая активность распространяется по предсердиям, она проходит через специализированные пути, известные как межузловые тракты , от узла SA к узлу AV .
АВ-узел и пучки: интервал PR
AV-узел функционирует как критическая задержка в проводящей системе. Без этой задержки предсердия и желудочки сокращались бы одновременно, и кровь не могла бы эффективно течь от предсердий к желудочкам. Задержка в АВ-узле формирует большую часть сегмента PR на ЭКГ , а часть реполяризации предсердий может быть представлена сегментом PR.
Дистальная часть АВ-узла известна как пучок Гиса . Пучок Гиса в межжелудочковой перегородке разделяется на две ветви: левую и правую. Левая ножка пучка Гиса активирует левый желудочек , а правая ножка пучка Гиса активирует правый желудочек .
Левая ножка пучка Гиса короткая, разделяется на левый передний пучок и левый задний пучок. Левый задний пучок относительно короткий и широкий, с двойным кровоснабжением, что делает его особенно устойчивым к ишемическим повреждениям. Левый задний пучок передает импульсы сосочковым мышцам, что приводит к закрытию митрального клапана. Поскольку левый задний пучок короче и шире правого, импульсы достигают папиллярных мышц непосредственно перед деполяризацией и, следовательно, сокращением миокарда левого желудочка. Это позволяет предварительно натянуть сухожильные хорды, увеличивая сопротивление потоку через митральный клапан во время сокращения левого желудочка. Этот механизм работает так же, как и предварительное натяжение автомобильных ремней безопасности.
Волокна Пуркинье / миокард желудочков: комплекс QRS
Две ветви пучка сужаются, образуя многочисленные волокна Пуркинье , которые стимулируют сокращение отдельных групп клеток миокарда.
Распространение электрической активности по миокарду желудочков приводит к возникновению комплекса QRS на ЭКГ .
Реполяризация предсердий происходит и маскируется во время комплекса QRS деполяризацией желудочков на ЭКГ .
Реполяризация желудочков
Последнее событие цикла — реполяризация желудочков . Это восстановление состояния покоя. На ЭКГ реполяризация включает точку J, сегмент ST и зубцы T и U.
Часть электрокардиограммы, измеренная трансторакально, PQRS, в основном зависит от симпатической нервной системы . На зубцы T (а иногда и U) в основном влияет парасимпатическая нервная система, управляемая интегрированным стволом мозга со стороны блуждающего нерва и грудных спинных дополнительных ганглиев .
Импульс ( потенциал действия ), который исходит из узла SA с относительной частотой 60–100 ударов в минуту, известен как нормальный синусовый ритм . Если узловые импульсы СА возникают с частотой менее 60 ударов в минуту, сердечный ритм известен как синусовая брадикардия . Если узловые импульсы СА возникают с частотой, превышающей 100 ударов в минуту, последующим учащением пульса является синусовая тахикардия . Однако эти состояния не обязательно являются плохими симптомами. Например, тренированные спортсмены обычно показывают частоту сердечных сокращений ниже 60 ударов в минуту, когда не тренируются. Если SA-узел не инициализируется, AV-соединение может взять на себя роль основного водителя ритма сердца. АВ-соединение состоит из АВ-узла, пучка Гиса и окружающей области; у него обычная скорость от 40 до 60 ударов в минуту. Эти «соединительные» ритмы характеризуются отсутствующим или инвертированным зубцом Р. Если и SA-узел, и AV-соединение не могут инициировать электрический импульс, желудочки могут сами генерировать электрические импульсы со скоростью от 20 до 40 ударов в минуту и будут иметь комплекс QRS более 120 мс. Это необходимо для того, чтобы сердце работало нормально.
Клиническая картина
Ортодромная тахикардия долгое время может протекать бессимптомно. Развитие приступа учащенного сердцебиения могут спровоцировать следующие факторы:
- Стрессовая ситуация;
- Резкий эмоциональный всплеск;
- Физическая перегрузка;
- Употребление спиртных напитков в больших дозах;
- Курение.
При возникновении приступа развивается следующая клиническая картина:
- Ощущение неритмичных сокращений сердца с последующим замиранием (признак экстрасистолы);
- Ощущение учащенного сердцебиения;
- Болевой синдром за грудиной различной интенсивности;
- Чувство нехватки воздуха, одышка, головокружение (признаки гипоксии);
- Кашель;
- Панические атаки, тремор рук;
- Резкая слабость, потемнение в глазах;
- Снижение АД.
При затяжном приступе и несвоевременном оказании неотложной помощи возможно развитие синкопального состояния (обморока).
Выраженность симптоматики ортодромной тахикардии зависит от следующих факторов:
- Степень увеличения ЧСС;
- Длительность пароксизмального приступа;
- Уровень артериального давления;
- Сократительная способность миокарда;
- Общее состояние организма.
Чаще всего приступ купируется самостоятельно с полным восстановлением сердечной деятельности.
Если пароксизмы возникают на фоне других сердечных патологий, возможно развитие недостаточности кровообращения.
Механизм развития
В основе механизма развития ортодромной тахикардии лежит нарушение ри. Оно подразумевает расщепление атриовентрикулярного (АВ) узла на несколько каналов:
- «Быстрый» канал, который находится в передней части АВ узла;
- «Медленный» канал – располагается в задней части АВ узла и представляет собой изолированные волокна.
Каждый канал имеет свои особенности проведения электроимпульсов: по одному из них они проходят быстро, по другому – медленно. Такая разница способствует возникновению дополнительной возбуждающей волны, которая провоцирует учащение сердцебиения.
Волна возбуждения проходит через предсердия, АВ узел, затем попадает в желудочки и через дополнительный путь проведения (пучок Кента) снова попадает в предсердия.
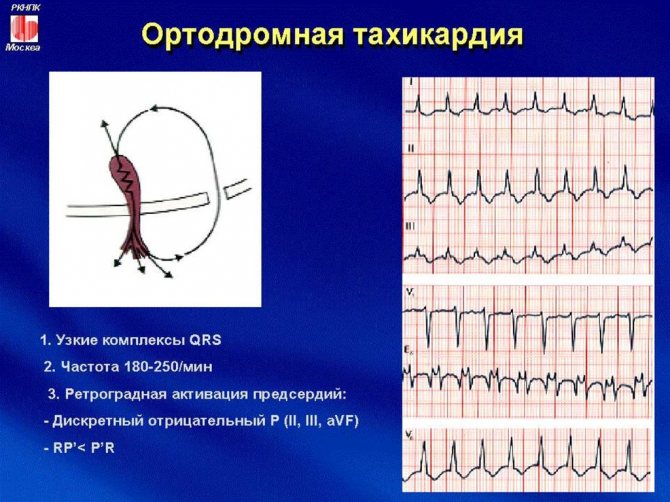
Реже встречается другое распространение волны возбуждения, которая имеет противоположную направленность: из предсердий импульс сразу попадает в патологический очаг (пучок Кента), из которого переходит в желудочки, а затем через АВ узел в предсердия.
Так возникает антидромная тахикардия, которая, в сравнении с ортодромной формой, встречается намного реже среди суправентрикулярных нарушениях ритма.
Возникновению ортодромной тахикардии присущи следующие этапы:
- Образование предсердной или желудочковой экстрасистолы;
- Формирование блокады «быстрого» канала;
- Передача импульса в желудочки через «медленный» канал;
- Восстановление работы «быстрого» канала;
- Ретроградная передача импульса из желудочков по «быстрому», а затем снова по «медленному» каналу.
Диагностика
Диагностика включает в себя целый ряд исследований, позволяющий судить как об общем состоянии организма, так и конкретно о деятельности сердца. Однако основным методом исследования, показывающим нарушение ритма, служит электрокардиограмма (ЭКГ).
ЭКГ-признаки
ЭКГ – это инструментальное диагностическое исследование, в ходе которого на тело и конечности накладываются специальные электроды, передающие информацию на ЭКГ-пленку. Этот метод позволяет судить об электрической активности сердца.
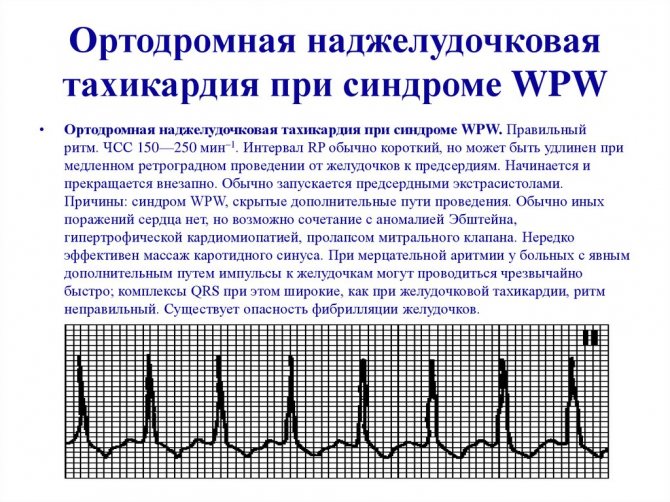
Основными ЭКГ-признаками ортодромной тахикардии являются:
- Комплексы QRS узкие, следуют друг за другом;
- Расстояние R-R укорачивается, но остается одинаковым;
- Предсердный зубец Р появляется в разных местах (как до, так и после желудочковых комплексов),
- Наслаивается на интервал S-T и зубец Т;
- Удлиненный интервал R-P.
Антидромная форма тахикардии на ЭКГ диагностируется при помощи следующих признаков:
- Желудочковые комплексы (QRS) широкие, по форме схожи с блокадой ножки пучка Гиса, расстояние между ними одинаковое;
- Наблюдается дельта-волна, которая обуславливает укорочение интервала P-Q;
- Зубец P наслаивается на комплекс QRS, может находиться после него.
Комплексная диагностика
Помимо ЭКГ назначаются и другие клинические и дополнительные исследования.
Клиническую диагностику осуществляет лечащий врач. Он применяет следующие методы:
- Сбор жалоб – диагностируются наиболее беспокоящие симптомы тахикардии;
- Сбор анамнеза – выясняется наличие факторов риска, вероятность отягощенной наследственности,
- Сопутствующих и фоновых заболеваний; большую роль в диагностике играет провоцирующие факторы, характер и длительность пароксизмов;
- Физикальный осмотр – оценивается состояние кожных покровов, деятельность основных систем организма;
- Измерение гемодинамических показателей – измерение АД и ЧСС;
- Аускультация сердца – оценка ритма сердца, характер сердечных тонов.
После сбора основной информации назначаются дополнительные исследования:
- Различные анализы крови (общее и биохимическое исследование, анализ на уровень гормонов) – назначается для выявления фоновых патологий;
- Суточное мониторирование ЭКГ – регистрация кардиограммы в течение суток с одновременным ведением дневника, в котором фиксируются эмоциональные и физические нагрузки, время бодрствования и сна;
- Назначается для диагностики провоцирующих факторов пароксизмов, а также их характеристик;
- Эхокардиография – УЗИ сердца, которое позволяет судить о наличии структурных изменений органа;
- Электрофизиологическое исследование – метод заключается в подаче к сердцу слабых доз тока для оценки его реакции и обнаружения скрытых патологий проводящей системы.

Проведение большого количества исследований необходимо для получения полной информации, постановки точного диагноза и определения тактики лечения.
Клетки первого типа
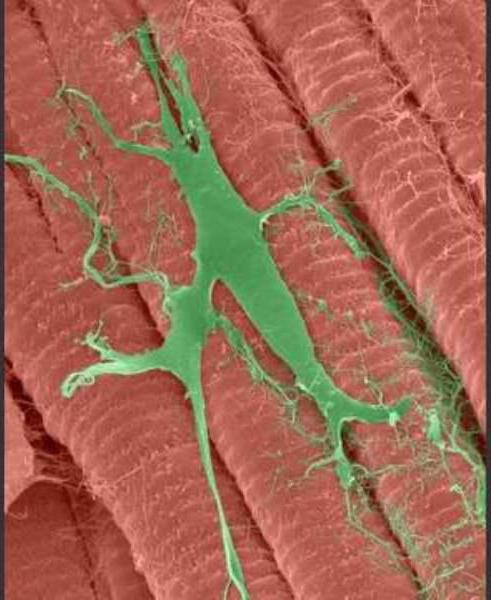
Различия клеток, которые входят в проводящую систему, связаны с тем, что они выполняют разные функции. Выделяют три основных типа клеток.
Ведущими водителями ритма являются П-клетки или клетки первого типа. Морфологически, это небольшие мышечные клетки, имеющие крупное ядро и много длинных отростков, переплетенных между собой. Несколько соседних клеток рассматриваются как кластер, объединенный общей базальной мембраной.
Для генерации сокращений во внутренней среде П-клеток расположены пучки миофибрилл. Эти элементы занимают не менее четверти от всего пространства цитоплазмы. Другие органеллы беспорядочно расположены внутри клетки и их меньше, чем в обычных кардиомиоцитах. А трубочки цитоскелета, наоборот, располагаются плотно и поддерживают форму водителей ритма.
Из этих клеток состоит сино-атриальный узел, но остальные элементы, в том числе и волокна Пуркинье (гистология которых будет описана ниже), имеют другое строение.
АТРИОВЕНТРИКУЛЯРНЫЙ УЗЕЛ
Атриовентрикулярный узел находится справа от межпредсердной перегородки над местом прикрепления створки трехстворчатого клапана, непосредственно рядом с устьем коронарного синуса. Форма и размеры его разные: в среднем длина его достигает 5-6 мм, а ширина — 2-3 мм.
Подобно синусовому узлу, атриовентрикулярный узел содержит также два вида клеток — Р и Т. Однако имеются значительные анатомические различия между синоаурикулярным и атриовентрикулярным узлами. В атриовентрикулярном узле гораздо меньше Р-клеток и незначительное количество сети коллагеновой соединительной ткани. У него нет постоянной, центрально проходящей артерии. В жировой клетчатке за атриовентрикулярным узлом, вблизи устья коронарного синуса, находится большое число волокон и ганглиев блуждающего нерва. Кровоснабжение атриовентрикулярного узла происходит посредством ramus septi fibrosi, называемой еще артерией атриовентрикулярного узла. В 90% случаев она отходит от правой венечной артерии, а в 10% — от ramus circumflexus левой венечной артерии.
Клетки атриовентрикулярного узла связываются анастомозами и образуют сетчатую структуру. В нижней части узла, перед переходом в пучок Гиса, клетки его располагаются параллельно друг другу.
Наджелудочковые тахикардии
Синусовая тахикардия
Источник ритма: синусовый узел. Может быть физиологической, но бывает и патологической — при ней сердце работает все еще ритмично, но слишком быстро (более 100-120 ударов в минуту).
Симптомы: боли в грудной клетке, затруднение дыхания, головокружения. Иногда протекает бессимптомно.
Лечение: физиологические варианты не нуждаются в терапии. При патологических вариантах до начала лечения рекомендовано пересмотреть образ жизни: увеличить объем потребляемой жидкости, повысить физическую активность и ограничить употребление веществ, стимулирующих сердце (кофе, крепкий чай, табак, алкоголь, медикаментозные средства). В качестве терапии используются бета-адреноблокаторы и антагонисты кальциевых каналов. Значительной опасности для жизни такая тахикардия не представляет.
Предсердные тахикардии
Источник ритма: чаще всего импульс возникает в правом предсердии около устьев сосудов и клапанов сердца, между синусовым и атриовентрикулярным узлами.
Симптомы: учащение сердцебиения до 150-200 ударов в минуту, одышка, дискомфорт и боль в области сердца, иногда предобморочные состояния.
Лечение: вагусные приемы (стимуляция блуждающего нерва, снижающего частоту сердечных сокращений), внутривенное введение антиаритмических препаратов. У пациентов с нестабильным кровообращением может проводиться синхронизированная электроимпульсная терапия (кардиоверсия-дефибрилляция — воздействие на миокард электрическим током, после чего ритм сердечной деятельности задает синусовый узел).
Атриовентрикулярные тахикардии
Источник ритма: АВ-узел. Импульс может распространяться вниз к желудочкам, вверх к предсердиям или в обоих направлениях одновременно.
Симптомы: одышка, потливость, головокружения вплоть до предобморочного и обморочного состояния, боль и/или дискомфорт в области сердца, ощущение пульсации в сосудах шеи и «дрожание рубашки» — сильные сокращения миокарда, способные передаться через грудную клетку на одежду.
Лечение: вагусные приемы, внутривенное введение антиаритмиков. Может понадобиться проведение кардиоверсии-дефибрилляции, установка кардиостимулятора, а также катетерная абляция (микрохирургическая процедура воздействия на аритмически активный участок миокарда радиочастотами; выполняется с помощью введенных внутрь сердца через сосуды катетеров).
Предсердные тахикардии выявляются у пациентов с ишемической болезнью, гипертонией, анатомическими пороками сердечных клапанов, миокардитами и кардиомиопатиями, то есть почти не встречаются у людей со здоровым сердцем.
Опасность наджелудочковых тахикардий заключаются в том, что на фоне основной патологии сердца тахикардия может перерасти в фибрилляцию предсердий — угрожающее жизни состояние.
Автоматизм клеток миокарда
Автоматизм — это способность специализированных клеток миокарда спонтанно вырабатывать электрические импульсы (син: потенциалы действия; ПД). Существует продольный (от предсердий к верхушке сердца) градиент автомата и проводящей системы. Принято различать три «центра» автоматизма:
1. синоатриальный узел — водитель ритма сердца первого порядка. В физиологических условиях этот узел генерирует импульсы с частотой 60-1 80 в мин;
2. атриовентрикулярный узел (клетки АВ-соединения) – водитель ритма сердца второго порядка, который способен генерировать 40—50 импульсов в 1 мин;
3. пучок Гиса (30—40 импульсов в 1 мин) и волокна Пуркинье (в среднем 20 импульсов в 1 мин) — водители ритма третьего порядка.
В норме единственным водителем ритма является синоатриальный узел, 1 который «не позволяет» реализоваться автоматической активности других потенциальных водителей ритма.
В основе автоматизма лежит медленная диастолическая деполяризация, постепенно понижающая мембранный потенциал до уровня порогового (критического) потенциала, с которого начинается быстрая регенеративная деполяризация мембраны, или фаза 0 потенциала действия.
Ритмичное возбуждение пейсмекерных клеток с частотой 70—80 в 1 мин можно объяснить двумя процессами: 1) ритмичным спонтанным повышением проницаемости мембран этих клеток для ионов Na+ и Са++, вследствие чего они поступают в клетку; 2) ритмичным снижением проницаемости для J ионов К+, в результате чего количество покидающих клетку ионов К+ уменьшается.
Согласно предложенному недавно альтернативному механизму, входящий пейсмекерный ток ионов Na+ (If) со временем возрастает, тогда как выходящий ток К+ остается неизменным. В целом данные процессы детерминируют развитие мед ленной диастолической деполяризации клеток пейс-мекера и достижение критического порога возбуждения (—40 мВ), обеспечивающего возникновение потенциала действия и его распространение по миокарду. Восходящая часть ПД клеток-пейсмекеров обеспечивается входом Са2+ в клетку Отсутствие плато можно объяснить характерным изменением проницаемости мембраны для ионов, при котором процессы деполяризации и инверсии плавно переходят в реполяризацию, которая также проходит более медленно из-за замедленного тока К+ из клетки. Амплитуда ПД составляет 70—80 мВ, его продолжительность — около 200 мс, рефрактерность — около 300 мс, те. длительность рефрактерного периода продолжительнее ПД, что защищает сердце от внеочередных импульсов (и соответственно преждевременного возбуждения), исходящих из других (как нормальных, так , и патологических) генераторов возбуждения, приходящихся на период не-возбудимости сердечной мышцы.
Функционирование дистальной (эффекторной) часта проводящей системы обеспечивают такие же процессы, которые происходят в клетках сино-атриального пейсмекера. В развитии спонтанной диастолической депаляризации в структурах системы Гиса—Пуркинье важную роль играет также ток ионов Na+ (И). Кроме того, в этом процессе участвуют и другие ионные токи, включая ток ионов К+ (ik), который в значительной степени определяет зависимость автоматизма волокон Пуркинье от внеклеточной концентрации ионов К+. При этом, отметим ток ионов К+ весьма незначителен в пейсмекерных клетках синоатриального узла, поскольку в них мало калиевых каналов.
В современной модели автоматизма волокон Пуркинье представлены четыре ионных механизма, зависящие от внеклеточной концентрации ионов К+:
1) активация тока ионов Na+ (If), усиливающая пейсмекерную активность;
2) активация тока ионов К+ (Ik), замедляющая или приостанавливающая пейсмекерную активность;
3) активация Na+/K+-Hacoca (Ip), замедляющая пейсмекерную активность;
4) уменьшение тока ионов K+(Ik), усиливающая пейсмекерную активность.
С электрофизиологической точки зрения, интервал между сокращениями сердца равен отрезку времени, в течение которого мембранный потенциал покоя в клетках-пейсмекерах синоатриального узла смещается до уровня порогового потенциала возбуждения
Существует строгая согласованность между процессом электрической активации каждого кардиомиоцита , возбуждением всего миокардиального синцития и сердечным циклом сердца.





